Door Maarten Veldhuizen
Moleculen zitten in een "vast" patroon in elkaar. om een paar voorbeelden te noemen: C(koolstof) die zit altijd viervoudig gebonden en H(waterstof) enkelvoudig gebonden (zoals bekent is uit het periodieke systeem)
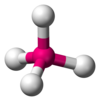 (zoals hier aangegeven CH4) deze is ook covalent.
(zoals hier aangegeven CH4) deze is ook covalent.Sommige moleculen zijn niet zo symmetrisch en kan het zijn dat ze één kan op gaan dat ligt aan de ladingen de de individuele atomen hebben (positief en negatief) dat word polair genoemd en dat kan je berekenen met het verschil van afzonderlijke atomen de EN-Waarde te vergelijken als dat verschil tussen de 0,4 en de 1,7 ligt. Dan zal de binding van atomen ook dichterbij de positieve liggen.
 dit is SO2 (het molecuul is als het ware "geknikt") het is een dipool
dit is SO2 (het molecuul is als het ware "geknikt") het is een dipool
Een hogere polariteit van een stof zorgt er voor dat het moeilijker uit elkaar gaat en daarmee zal die pas later gaat koken.(Het kan zijn van een stof die heel laag kookpunt heeft en die iets hoger wordt.)
Bronvermelding: Werkboek Scheikunde & www.Wikipedia.nl
Vragen:
Teken minimaal 3 moleculen uit deze rij.(geef ook de polaire binding aan waar nodig) H2, H2O, NH3, HCl, NO2, IF4
Dank je wel Maarten, je stuk ziet erg goed verzorgt en is inhoudelijk precies wat ik bedoel
BeantwoordenVerwijderentot morgen en groeten,
Joost
Tip: is mis een paragraaf!
BeantwoordenVerwijderen