http://phet.colorado.edu/en/simulation/molecule-polarity
Dit is onze opdracht 3.
Het gaat over dipolen en aantrekkingskracht van de atomen.
LMA1cdGroep15
Dit is de LMA1cd groep 15 van Chemie van school
vrijdag 16 maart 2012
maandag 12 maart 2012
Vragen voor opdracht 2
Vragen Hoofdstuk 7.1 t /m 7.3 & 'Zouten'
1 Wat zijn zouten?
2 Geef de verhoudingsformules van,
zilversulfide
calciumfluoride
3 Geef de verhoudingsformules van,
kaliumfosfaat
calciumoxide
aluin
4 Noem vier metaaloxiden die met water reargeren
en benoem van elk de triviale naam.
5 Wat gebeurt er als je het zout(CuS) oplost?
6 Teken het ionrooster van Na+ en Cl-.
7 Geef de reactie van ijzer en chloor tot ijzer(III)chloride
8 Hoeveel gram kan er ongeveer opgelost worden in 1 liter in:
a) een goed oplosbare stof
b) een matig oplosbare stof
c) een slecht oplosbare stof
d) geef ook een voorbeeld van een slecht & goed oplosbare stof
1 Wat zijn zouten?
2 Geef de verhoudingsformules van,
zilversulfide
calciumfluoride
3 Geef de verhoudingsformules van,
kaliumfosfaat
calciumoxide
aluin
4 Noem vier metaaloxiden die met water reargeren
en benoem van elk de triviale naam.
5 Wat gebeurt er als je het zout(CuS) oplost?
6 Teken het ionrooster van Na+ en Cl-.
7 Geef de reactie van ijzer en chloor tot ijzer(III)chloride
8 Hoeveel gram kan er ongeveer opgelost worden in 1 liter in:
a) een goed oplosbare stof
b) een matig oplosbare stof
c) een slecht oplosbare stof
d) geef ook een voorbeeld van een slecht & goed oplosbare stof
dinsdag 6 maart 2012
Samenvatting van hoofdstuk 6,7:Ruimtelijke bouw Door Maarten Veldhuizen
Samenvatting van Hoofdstuk 6,7: Ruimtelijke bouw
Door Maarten Veldhuizen
Moleculen zitten in een "vast" patroon in elkaar. om een paar voorbeelden te noemen: C(koolstof) die zit altijd viervoudig gebonden en H(waterstof) enkelvoudig gebonden (zoals bekent is uit het periodieke systeem)
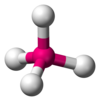 (zoals hier aangegeven CH4) deze is ook covalent.
(zoals hier aangegeven CH4) deze is ook covalent.
Sommige moleculen zijn niet zo symmetrisch en kan het zijn dat ze één kan op gaan dat ligt aan de ladingen de de individuele atomen hebben (positief en negatief) dat word polair genoemd en dat kan je berekenen met het verschil van afzonderlijke atomen de EN-Waarde te vergelijken als dat verschil tussen de 0,4 en de 1,7 ligt. Dan zal de binding van atomen ook dichterbij de positieve liggen.
 dit is SO2 (het molecuul is als het ware "geknikt") het is een dipool
dit is SO2 (het molecuul is als het ware "geknikt") het is een dipool
Bronvermelding: Werkboek Scheikunde & www.Wikipedia.nl
Vragen:
Teken minimaal 3 moleculen uit deze rij.(geef ook de polaire binding aan waar nodig) H2, H2O, NH3, HCl, NO2, IF4
Door Maarten Veldhuizen
Moleculen zitten in een "vast" patroon in elkaar. om een paar voorbeelden te noemen: C(koolstof) die zit altijd viervoudig gebonden en H(waterstof) enkelvoudig gebonden (zoals bekent is uit het periodieke systeem)
 (zoals hier aangegeven CH4) deze is ook covalent.
(zoals hier aangegeven CH4) deze is ook covalent.Sommige moleculen zijn niet zo symmetrisch en kan het zijn dat ze één kan op gaan dat ligt aan de ladingen de de individuele atomen hebben (positief en negatief) dat word polair genoemd en dat kan je berekenen met het verschil van afzonderlijke atomen de EN-Waarde te vergelijken als dat verschil tussen de 0,4 en de 1,7 ligt. Dan zal de binding van atomen ook dichterbij de positieve liggen.
 dit is SO2 (het molecuul is als het ware "geknikt") het is een dipool
dit is SO2 (het molecuul is als het ware "geknikt") het is een dipool
Een hogere polariteit van een stof zorgt er voor dat het moeilijker uit elkaar gaat en daarmee zal die pas later gaat koken.(Het kan zijn van een stof die heel laag kookpunt heeft en die iets hoger wordt.)
Bronvermelding: Werkboek Scheikunde & www.Wikipedia.nl
Vragen:
Teken minimaal 3 moleculen uit deze rij.(geef ook de polaire binding aan waar nodig) H2, H2O, NH3, HCl, NO2, IF4
zondag 4 maart 2012
Samenvatting hoofdstuk 6.8
Door Bram Derksen
Vanderwaalskrachten zijn zwakke aantrekkende krachten tussen de molekulen.
Bij een lagere temperatuur zijn de vanderwaalskrachten sterk genoeg om de molekulen bij elkaar te houden. Dit is het geval in de vaste fase.
Als de temperatuur verhoogt wordt gaan de molekulen bewegen (trillen op een vaste plaats).
De beweging kan zo hefig worden dat de molekulen elkaar niet meer op de plaats kunnen houden en langs elkaar gaan bewegen. De stof wordt dan vloeibaar.
De sterkte van de vanderwaalskracht hangt af van:
molekuulmassa: hoe groter de molekulen (dus hoe groter de molekuulmassa) hoe sterker de vanderwaalskracht.
aantal elektronen: hoe meer elektronen in de molekulen voorkomen hoe sterker de vanderwaalskracht.
Een molekuulrooster is: moleculaire stoffen in een vaste toestand in constante rangschikking.
Moleculaire stoffen zijn stoffen die alleen bestaan uit niet-metaalatomen.
De molekulen worden in het rooster door de zwakke vanderwaalskracht bij elkaar gehouden, terwijl er in de molekulen sprake is van sterkere atoombindingen.
Door de zwakke binding tussen de molekulen smelten stoffen met een molekuulrooster al bij vrij lage temperaturen.
Tot de stoffen met molekuulroosters behoren vrijwel alle stoffen waarin geen metalen voorkomen, bijvoorbeeld vele organische stoffen zoals suiker en vet.
Alle stoffen die onder normale omstandigheden in de gasfase voorkomen zijn molekulaire stoffen,
bijvoorbeeld zuurstof en ammoniak.
Ook bijna alle vloeistoffen zijn molekulair zoals bijvoorbeeld water.
Vaste stoffen waarvan het smeltpunt lager is dan 300 graden celcius, zijn meestal ook molekulaire stoffen.
Vragen.
1: Leg in eigen woorden uit wat je verstaat onder vanderwaalskrachten en molekuulrooster.
2: Waarmee hangt de sterkte van de vanderwaalskrachten samen?
Bronvermelding.
Ons chemie boek.
Scheikunde voor het laboratorium onderwijs.
Door Bram Derksen
Vanderwaalskrachten zijn zwakke aantrekkende krachten tussen de molekulen.
Bij een lagere temperatuur zijn de vanderwaalskrachten sterk genoeg om de molekulen bij elkaar te houden. Dit is het geval in de vaste fase.
Als de temperatuur verhoogt wordt gaan de molekulen bewegen (trillen op een vaste plaats).
De beweging kan zo hefig worden dat de molekulen elkaar niet meer op de plaats kunnen houden en langs elkaar gaan bewegen. De stof wordt dan vloeibaar.
De sterkte van de vanderwaalskracht hangt af van:
molekuulmassa: hoe groter de molekulen (dus hoe groter de molekuulmassa) hoe sterker de vanderwaalskracht.
aantal elektronen: hoe meer elektronen in de molekulen voorkomen hoe sterker de vanderwaalskracht.
Een molekuulrooster is: moleculaire stoffen in een vaste toestand in constante rangschikking.
Moleculaire stoffen zijn stoffen die alleen bestaan uit niet-metaalatomen.
De molekulen worden in het rooster door de zwakke vanderwaalskracht bij elkaar gehouden, terwijl er in de molekulen sprake is van sterkere atoombindingen.
Door de zwakke binding tussen de molekulen smelten stoffen met een molekuulrooster al bij vrij lage temperaturen.
Tot de stoffen met molekuulroosters behoren vrijwel alle stoffen waarin geen metalen voorkomen, bijvoorbeeld vele organische stoffen zoals suiker en vet.
Alle stoffen die onder normale omstandigheden in de gasfase voorkomen zijn molekulaire stoffen,
bijvoorbeeld zuurstof en ammoniak.
Ook bijna alle vloeistoffen zijn molekulair zoals bijvoorbeeld water.
Vaste stoffen waarvan het smeltpunt lager is dan 300 graden celcius, zijn meestal ook molekulaire stoffen.
Vragen.
1: Leg in eigen woorden uit wat je verstaat onder vanderwaalskrachten en molekuulrooster.
2: Waarmee hangt de sterkte van de vanderwaalskrachten samen?
Bronvermelding.
Ons chemie boek.
Scheikunde voor het laboratorium onderwijs.
Abonneren op:
Reacties (Atom)